Resumen
Antecedentes
El asma es una enfermedad crónica común de las vías respiratorias en todo el mundo que no se puede curar y genera una enorme carga para la salud pública. El estrés oxidativo se consideró un mecanismo importante en la patogenia del asma. Se ha demostrado que el gas hidrógeno funciona como un nuevo antioxidante y ejerce una actividad antioxidante terapéutica en varias enfermedades y la función de este gas no tóxico en el asma no estaba clara. El propósito del estudio tiene como objetivo examinar el efecto de la inhalación de gas hidrógeno en la fisiopatología de un modelo de asma en ratones.
Métodos
En este estudio se utilizó un modelo murino de inflamación alérgica de las vías respiratorias inducida por ovoalbúmina (OVA). Brevemente, los ratones se sensibilizaron a la ovoalbúmina y recibieron una inhalación de una alta concentración de gas hidrógeno al 67 % durante 60 min una vez al día durante 7 días consecutivos después de la provocación con OVA o PBS, respectivamente. La función pulmonar se evaluó en el aparato con 4 canales de sistema de señales biológicas. La morfología y la hiperplasia de las células caliciformes se tiñeron mediante H/E y tinción con ácido peryódico de Schiff. La clasificación citológica en el líquido de lavado alveolar bronquial (BALF) se analizó mediante tinción de Wright Giemsa. Se recogieron suero, BALF y tejido pulmonar para ensayo bioquímico. Se utilizó el análisis de varianza de una vía (ANOVA) para determinar la significación estadística entre los grupos. Las comparaciones múltiples se realizaron mediante la prueba de comparación múltiple de Bonferroni utilizando el software GraphPad Prism 5.
Resultados
La inhalación de gas hidrógeno anuló la ovoalbúmina inducida por el aumento de la resistencia pulmonar. Al mismo tiempo, los ratones asmáticos mostraron una infiltración inflamatoria grave e hiperplasia de células caliciformes que se revirtieron mediante la inhalación de gas hidrógeno. La inhalación de gas hidrógeno redujo significativamente el número total de células, eosinófilos y linfocitos en BALF. El aumento del nivel de IL-4, IL-13, TNF-α y CXCL15 en BALF e IL-4 en el suero disminuyó significativamente después de la inhalación. La inhalación de gas hidrógeno aumentó notablemente la actividad de la superóxido dismutasa disminuida y atenuó significativamente el nivel aumentado de malondialdehído y mieloperoxidasa.
Conclusiones
La inhalación de gas hidrógeno mejora la función pulmonar y protege la inflamación establecida de las vías respiratorias en el modelo de ratones asmáticos alérgicos que puede estar asociado con la inhibición del proceso de estrés oxidativo. Este estudio proporciona una potencial oportunidad terapéutica alternativa para el manejo clínico del asma.
Antecedentes
El asma es una enfermedad respiratoria crónica común con una mayor prevalencia, lo que resulta en una pesada carga para la salud pública en todo el mundo. Esta desafiante enfermedad caracterizada por una inflamación persistente de las vías respiratorias no se puede curar. Aunque se han hecho muchos esfuerzos para aumentar el efecto terapéutico. El estrés oxidativo juega un papel importante en la patogenia de este trastorno crónico. La inflamación induce una reacción de estrés oxidativo pulmonar y conduce a una gran cantidad de especies reactivas de oxígeno. [1]. El efecto de las especies reactivas de oxígeno en la patogenia del asma es estimular el deterioro de la función pulmonar, la desgranulación de los mastocitos, la remodelación de las vías respiratorias y la secreción de moco por el epitelio, todo lo cual a su vez puede agravar la inflamación local del pulmón.
El hidrógeno se considera un gas inerte y se ha utilizado en aplicaciones médicas para prevenir la enfermedad por descompresión en buceadores profundos. [2]. En 2007 se informó que el hidrógeno administrado por inhalación tiene auténticas propiedades antioxidantes y antiapoptóticas que pueden proteger el cerebro contra la lesión por isquemia/reperfusión al neutralizar selectivamente los radicales hidroxilo. [3]. Este informe despertó un interés considerable en todo el mundo. Se han investigado los efectos terapéuticos del hidrógeno molecular en diversas enfermedades en relación con su capacidad antioxidante. [4] y su antiinflamatorio [5] y anti-apoptosis [6] capacidades. En comparación con los antioxidantes tradicionales, el hidrógeno es una molécula pequeña que puede disiparse fácilmente por todo el cuerpo y las células, y es lo suficientemente suave como para no alterar las reacciones metabólicas de oxidación-reducción o la señalización celular mediada por ROS. Por lo tanto, puede ser un antioxidante seguro y eficaz para las enfermedades pulmonares. Como vía principal de administración, la inhalación se considera el método preferido en el tratamiento del asma. Recientemente, la evidencia acumulada ha demostrado varios tipos de enfermedades relacionadas con el estrés oxidativo, incluida la cardiopatía isquémica [7]carrera [8]lesión pulmonar aguda [9] y enfermedad inflamatoria intestinal [5], se beneficiaron o fueron protegidos por la inhalación de gas hidrógeno. El efecto de este tipo de gas sobre el asma no se comprende completamente. Por lo tanto, el objetivo de este estudio fue investigar la función antiinflamatoria y antioxidante de la inhalación de altas concentraciones de gas hidrógeno en un modelo asmático de ratón.
Métodos
animales
Se alojaron ratones BALB/c adquiridos en el Centro de Animales Experimentales de la Segunda Universidad Médica Militar en habitaciones mantenidas a temperatura constante (21 ± 2 °C) y humedad (55 ± 15 %) con un ciclo de luz/oscuridad de 12 h y se les permitió comer. y agua ad libitum. Se utilizaron ratones hembra de 6 a 8 semanas de edad para los experimentos. Cuarenta ratones se dividieron al azar en cuatro grupos con 10 ratones cada uno: grupo de control simulado (Control, C), grupo de asma (A), grupo de tratamiento con gas hidrógeno (AH) y grupo de control con gas hidrógeno (Hidrógeno, H). El experimento se repitió tres veces. Los protocolos experimentales fueron aprobados por el Comité Ético de Estudios en Animales de la Segunda Universidad Médica Militar, Shanghái, China.
Sensibilización con ovoalbúmina (OVA)/desafío con aerosol
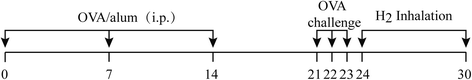
Se prepararon modelos de ratón de asma con sensibilización y exposición a OVA de pollo. Brevemente, 20 μg (100 μl) de OVA de pollo que se emulsionó con alumbre (2,25 mg Al(OH)32 mg Mg(OH)2; Pierce, EE. UU.) se inyectó por vía intraperitoneal en ratones los días 0, 7 y 14. La provocación de las vías respiratorias se proporcionó mediante un aerosol de solución salina sola u OVA al 1 % (0,01 g/ml) en solución salina generada por nebulización ultrasónica (DeVilbiss, EE. UU.), que los ratones inhalaron durante 20 min los días 21, 22 y 23. Los ratones de los grupos AH y H se trataron inhalando una alta concentración de hidrógeno gaseoso (67 %) durante 60 min una vez al día durante 7 días consecutivos después de la OVA y desafío con PBS, respectivamente (Fig. 1). Los ratones fueron anestesiados con una sobredosis de hidrato de cloral ip seguida de exanguinación 24 h después del último tratamiento.
Administración de gas hidrógeno
El gas mixto que consta de 67% H2 y 33% O2 fue producido por el nebulizador de oxígeno de hidrógeno AMS-H-01 (Asclepius, Shanghai, China), que fue diseñado específicamente para extraer el hidrógeno y el oxígeno del agua. Los ratones se colocaron en una caja cerrada transparente (20 × 18 × 15 cm, largo x ancho x alto) en la que se introdujo el gas mixto a razón de 200 ml/min durante todo el experimento. La caja se lavó con una mezcla de gases durante 30 min para reemplazar el aire de la caja. Durante cada experimento, la concentración de hidrógeno gaseoso en la caja se controló mediante cromatografía de ultragases Thermal Trace GC (Thermo Fisher, MA, EE. UU.).
Medición de la función pulmonar
La función pulmonar se evaluó en el aparato con 4 canales de sistema de señales biológicas (Modelo SMUP-PC, Universidad de Fudan). Los ratones se anestesiaron ip con hidrato de hidracina, se traqueotomizaron con una cánula roma de calibre 18 y se ventilaron. El flujo de gas se determinó y registró mediante el transductor de flujo de aire Fleisch conectado con la intubación de la tráquea en condiciones de respiración espontánea del ratón. La presión dentro del esófago se puede registrar continuamente como presión en el pecho. La resistencia pulmonar (RL) y la distensibilidad dinámica del sistema respiratorio (Cdyn) se calcularon por el método de Amdur y Mead de acuerdo con la frecuencia respiratoria, el volumen corriente, el flujo respiratorio y la presión torácica [10].
Recolección y preparación de tejidos.
El lavado broncoalveolar (BAL) se realizó después de las mediciones de hiperreactividad de las vías respiratorias cuando el animal aún estaba bajo anestesia. Se usó un volumen total de 0,5 ml de PBS frío para lavar los pulmones tres veces. La sangre se recogió mediante punción cardíaca con una aguja de calibre 20 y el suero se preparó mediante centrifugación en tubos de suero y se almacenó a -20 °C para análisis posteriores. Los ratones fueron sacrificados con dislocación cervical. Se extrajo el lóbulo del pulmón izquierdo y se fijó en formaldehído al 4% durante la noche. Los lóbulos superior y medio del pulmón derecho se congelaron instantáneamente en hielo seco y se almacenaron a -80 °C hasta su posterior procesamiento. La proteína se extrajo de las muestras ultracongeladas de tejido pulmonar con un kit de lisis celular (Bio-plexTM Cell Lysis kit, Bio-Rad) suplementado con inhibidores de proteinasa (Sigma-Aldrich).
Evaluación de la histología pulmonar
Después de una preparación adecuada, se tiñeron secciones de parafina de 5 μm de espesor del pulmón izquierdo con hematoxilina y eosina (H&E) para evaluar la morfología general. Los grados de inflamación pulmonar de cinco secciones de las vías respiratorias distribuidas aleatoriamente por todo el pulmón izquierdo fueron evaluados por un analista cegado a los grupos utilizando una escala subjetiva que va de 0 a 4 (0, normal; 1, leve; 2, moderado; 3, grave; 4, más grave). Se aplicó tinción con ácido peryódico de Schiff (PAS) para detectar mucosustancias. Las imágenes de tejidos pulmonares con vías respiratorias fueron capturadas por un microscopio Nikon. Se calcularon el área positiva para PAS y el área total del epitelio bronquial correspondiente, y el sistema de clasificación adoptado fue: 0, sin células caliciformes; 1, <15%; 2, 15-30%; 3, 30-45%; 4, 45-60%; 5, > 60% [11].
Índice de estrés oxidativo en tejido pulmonar
Una parte de la preparación de tejido se hizo a partir de tejido de pulmón derecho que se homogeneizó con solución salina normal y la preparación se centrifugó a 2500 rpm a 4 °C durante 10 min. El sobrenadante resultante se equilibró con solución salina y se usó para determinar los niveles de proteínas en los homogeneizados de tejido. Los niveles de superóxido dismutasa (SOD), glutatión (GSH), catalasa (CAT), malondialdehído (MDA), mieloperoxidasa (MPO) y 8-hidroxideoxiguanosina (8-OHdG) se determinaron utilizando kits comerciales (Nanjing Jiancheng, Nanjing, China ). Las determinaciones se realizaron estrictamente de acuerdo con las instrucciones del fabricante.
Citocina en líquido de lavado alveolar bronquial (BALF) y suero
Se utilizó un ensayo inmunoabsorbente ligado a enzimas (ELISA) (R&D Systems, Minneapolis, MN, EE. UU.) para determinar los niveles de expresión de IL-4, IL-5, IL-13, IL-6, TNF-α y CXCL15 en BALF y suero de acuerdo con las instrucciones del fabricante. La absorbancia se midió a 450 nm utilizando un lector de microplacas (Modelo 680; Bio-Rad, Hercules, CA, EE. UU.).
análisis estadístico
Para el análisis estadístico se utilizó el software GraphPad Prism 5. Los datos de todos los ratones de cada grupo se presentaron como las medias ± SD o la mediana (rango intercuartil [IQR]) para variables continuas. Se utilizó el análisis de varianza de una vía (ANOVA) para determinar la significación estadística entre los grupos. Las comparaciones múltiples se realizaron mediante la Prueba de Comparación Múltiple de Bonferroni. PAGS< 0,05 se consideró estadísticamente significativo.
Resultados
La inhalación de gas hidrógeno disminuyó la resistencia pulmonar en el modelo de ratones asmáticos
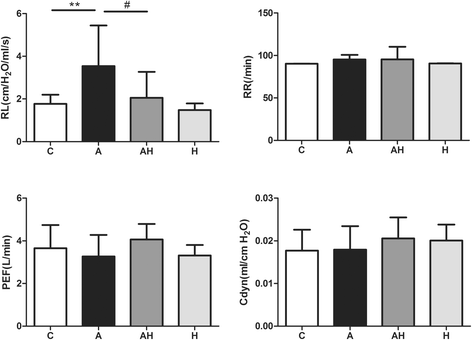
La resistencia pulmonar (RL) aumentó en el modelo de ratón asmático (3,537 ± 1,9 cm/H2O/ml/s vs 1,765 ± 0,43 cm/H2O/ml/s, PAGS< 0,01) en comparación con el grupo control y fue significativamente menor en el grupo AH en comparación con el grupo A (2,052 ± 1,2 cm/H2O/ml/s frente a 3,53 ± 1,9 cm/H2O/ml/s, PAGS< 0,05) (fig. 2). No hubo diferencias significativas en la frecuencia respiratoria (RR), la tasa de flujo máximo (PEF) y el cumplimiento dinámico (Cdyn) (Fig. 2) entre los cuatro grupos.
El efecto de la inhalación de gas hidrógeno en la función pulmonar en el modelo de ratón asmático. C: grupo control (norte= 10), A: grupo asma (norte= 10), AH: grupo de asma más inhalación de gas hidrógeno (norte= 10), H: grupo control más inhalación de gas hidrógeno (norte= 10). **: vs grupo de control, PAGS<0,01; #: vs grupo de asma, PAGS<0.05