Resumen
Antecedentes
La EPOC está asociada con el desarrollo de cáncer de pulmón. El efecto protector de los corticosteroides inhalados (ICS) sobre el cáncer de pulmón aún es controvertido. Por lo tanto, este estudio investigó el desarrollo de cáncer de pulmón según la prescripción de inhaladores y las comorbilidades en la EPOC.
Métodos
Se realizó un estudio de cohorte retrospectivo basado en la base de datos del Servicio de Evaluación y Revisión de Seguros de Salud de Corea. Se investigó el desarrollo de cáncer de pulmón desde la fecha de índice hasta el 31 de diciembre de 2020. Esta cohorte incluyó pacientes con EPOC (≥ 40 años) con nueva prescripción de inhaladores. Se excluyeron los pacientes con antecedentes de cualquier cáncer durante el período de selección o un cambio de inhalador después de la fecha de índice.
Resultados
De los 63.442 pacientes elegibles, 39.588 pacientes (62,4%) estaban en el grupo de antagonistas muscarínicos de acción prolongada (LAMA) y agonistas β2 de acción prolongada (LABA), 22.718 (35,8%) en el grupo de ICS/LABA y 1.136 (1,8%) en el grupo de LABA. El análisis multivariado no mostró diferencias significativas en el desarrollo de cáncer de pulmón según la prescripción del inhalador. El análisis multivariado, ajustado por edad, sexo y factores significativos en el análisis univariado, demostró que la enfermedad pulmonar intersticial difusa (EPID) (HR = 2,68; IC del 95 % = 1,86-3,85), una puntuación más alta en el índice de comorbilidad de Charlson (HR = 1,05; IC del 95 % = 1,01-1,08) y dos o más hospitalizaciones durante el período de selección (HR = 1,19; IC del 95 % = 1,01-1,39), junto con una edad avanzada y el sexo masculino, se asociaron de forma independiente con el desarrollo de cáncer de pulmón.
Conclusión
Nuestros datos sugieren que el desarrollo de cáncer de pulmón no está asociado independientemente con la prescripción de inhaladores, sino con la EPID coexistente, una puntuación más alta en el índice de comorbilidad de Charlson y una hospitalización frecuente.
Introducción
Varios estudios epidemiológicos sugieren una estrecha asociación entre la enfermedad pulmonar obstructiva crónica (EPOC) y el cáncer de pulmón (1,2,3,4). La EPOC, incluso en los que nunca han fumado, se asocia con cáncer de pulmón, y la presencia de EPOC en fumadores se asocia con un riesgo dos a seis veces mayor de desarrollar cáncer de pulmón (1, 5, 6).
Los mecanismos patogénicos de la asociación entre la EPOC y el cáncer de pulmón incluyen el tabaquismo, la mayor expresión de factores de crecimiento en la EPOC, la inflamación crónica, la predisposición genética, el mecanismo epigenético y el envejecimiento prematuro.7, 8). Además, se informa que algunas comorbilidades, como la diabetes mellitus y la tuberculosis en la EPOC, son factores de riesgo de cáncer de pulmón (6, 9).
Recientemente, se ha sugerido el tratamiento farmacológico con corticosteroides inhalados (ICS) como una estrategia para reducir el riesgo de cáncer de pulmón, ya que la inflamación crónica en la EPOC promueve el crecimiento tumoral y suprime las respuestas inmunes antitumorales (10, 11). Los metanálisis retrospectivos han demostrado que los ICS reducen el riesgo de cáncer de pulmón en la EPOC, aunque la calidad de la evidencia es baja (12, 13). Sin embargo, algunos estudios no lograron confirmar el vínculo entre los ICS y el cáncer de pulmón (13, 14). Los sesgos relacionados con el tiempo, incluidos el sesgo de tiempo inmortal, el sesgo de tiempo de latencia y el sesgo protopático, no se tuvieron en cuenta por completo en estudios anteriores, lo que dio lugar a resultados contradictorios. Además, aún quedan por determinar los efectos de otras terapias antiinflamatorias, incluida la terapia con antagonistas muscarínicos de acción prolongada (LAMA) y la terapia con agonistas β2 de acción prolongada (LABA), sobre el desarrollo de cáncer de pulmón en la EPOC.
Investigamos el desarrollo de cáncer de pulmón en pacientes con EPOC según la prescripción de inhaladores y las comorbilidades mediante el análisis de la base de datos del Servicio de Evaluación y Revisión de Seguros Médicos de Corea (HIRA). El diseño del estudio utilizado tuvo en cuenta los sesgos relacionados con el tiempo, para proporcionar más información sobre los riesgos de desarrollo de cáncer de pulmón utilizando un tamaño de muestra grande.
Materiales y métodos
Diseño del estudio
Este estudio analizó los datos de la base de datos HIRA desde el 1 de enero de 2015 hasta el 31 de diciembre de 2020. La base de datos HIRA contiene registros de reclamaciones de servicios médicos que incluyen todos los diagnósticos y medicamentos de todos los entornos de atención médica para casi toda la población coreana bajo el seguro médico nacional obligatorio y universal.
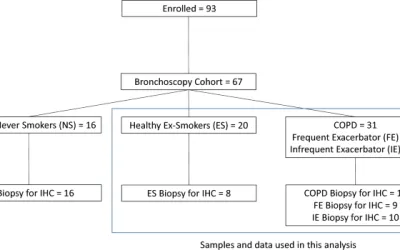
La cohorte de EPOC de la base de datos HIRA se construyó según los siguientes criterios: (1) pacientes ≥ 40 años, (2) al menos tres visitas ambulatorias separadas, (3) EPOC (códigos J43⎼J44 de la Clasificación Internacional de Enfermedades, décima revisión (CIE-10)) como diagnóstico principal desde el 1 de enero de 2015 hasta el 31 de diciembre de 2020, con prescripción de uno de los siguientes medicamentos respiratorios: LAMA, LABA, combinación de LAMA/LABA, ICS, combinación de ICS/LABA, triple terapia (LAMA + LABA + ICS), inhibidores de la fosfodiesterasa-4, teofilina y mucolíticos (Fig. 1). Para ser incluido en cada grupo de inhaladores se requirieron tres o más prescripciones de un inhalador durante el período de exposición. El uso de corticosteroides orales (OCS) se identificó como la prescripción de prednisolona 420 mg (15 mg/día durante cuatro semanas) o más para EPOC durante el período de exposición.
Figura 1Diagrama de flujo de la población de estudio. Abreviaturas: CCI = puntuación del índice de comorbilidad de Charlson; EPOC = enfermedad pulmonar obstructiva crónica; HIRA = Servicio de revisión y evaluación de seguros de salud; ICS = corticosteroide inhalado; LABA = agonista beta de acción prolongada; LAMA = antagonista muscarínico de acción prolongada
Imagen de tamaño completoCada paciente tuvo un período de detección de un año sin ningún medicamento inhalador antes de la fecha índice. La fecha índice se definió como la fecha de la primera prescripción de medicamento inhalador. Se estableció un período de latencia antes del diagnóstico de cáncer de pulmón para permitir tiempo suficiente para la exposición al inhalador con respecto al desarrollo del cáncer, como en otros estudios (14, 15) (Higo. 2).
Figura 2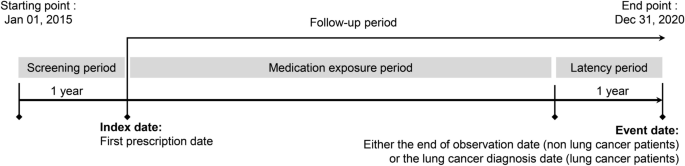
Diseño del estudio. Los medicamentos recibidos durante el período de latencia entre la exposición al medicamento y el diagnóstico de cáncer de pulmón no se contabilizaron como exposiciones.
Imagen de tamaño completoDurante el período de selección, se excluyó a los sujetos que tenían antecedentes de cáncer o a quienes se les había recetado un inhalador. También se excluyó a los pacientes a quienes se les había recetado un inhalador después de la fecha de inicio.
Esta cohorte consistió en tres grupos: 1) grupo LAMA/LABA como LAMA + LABA o combinación de dosis fija LAMA/LABA, 2) grupo ICS/LABA como ICS + LABA o combinación de dosis fija ICS/LABA, 3) grupo LABA que utilizó un inhalador LABA solo. Los sujetos fueron monitoreados para el diagnóstico de cáncer de pulmón desde el 1 de enero de 2016 hasta el 31 de diciembre de 2020 (Fig. 2).
Identificación de casos
Los casos de cáncer de pulmón (C33-C34) se identificaron mediante códigos CIE-10 después de la prescripción inicial de inhaladores. También se identificaron comorbilidades según los siguientes códigos CIE-10: asma (J45-46), hipertensión (I10-15), diabetes mellitus (E10-E14), enfermedad pulmonar intersticial difusa (EPID) (J84), cardiopatía isquémica (I20-I25), insuficiencia cardíaca (I50), enfermedad cerebrovascular (I60-I69) y tromboembolia pulmonar (I26). La fecha del evento fue la primera fecha de diagnóstico de cáncer según los códigos CIE-10 anteriores. Se excluyeron los pacientes en los que se diagnosticó cáncer de pulmón en el período de latencia después de la prescripción inicial.
Ajuste por covariables
Se realizaron análisis de modelos multivariados que incluían covariables que afectaban el riesgo de desarrollar cáncer. Se realizó un ajuste por la gravedad de la EPOC utilizando el índice de comorbilidad de Charlson y el número de visitas a la sala de emergencias y hospitalizaciones. Los análisis multivariados incluyeron dos modelos: el modelo 1 tenía todas las covariables y el modelo 2 tenía covariables que incluían edad, sexo y factores significativos en el análisis univariado.
análisis estadístico
Las características basales y la prescripción de medicamentos se resumieron mediante estadísticas descriptivas que incluyeron media, desviación estándar y proporción. Se utilizó una prueba de chi-cuadrado para las variables categóricas y un análisis de varianza (ANOVA) unidireccional para las variables continuas. La prevalencia de cáncer de pulmón entre los tres grupos según la terapia con inhaladores se evaluó mediante una prueba de chi-cuadrado y se ajustó mediante una corrección de Bonferroni para comparaciones múltiples. La tasa de incidencia de cáncer de pulmón por 10 000 personas-año se calculó con intervalos de confianza (IC) del 95 % y se comparó con el análisis de regresión de Poisson. El supuesto de riesgo proporcional se analizó utilizando residuos de Schoenfeld para el modelo de regresión de riesgos proporcionales de Cox. Se utilizaron análisis de regresión de riesgos proporcionales de Cox univariados y multivariados para identificar factores de riesgo significativos que predicen el desarrollo de cáncer de pulmón.
Se realizaron análisis de sensibilidad estableciendo períodos de latencia de 6, 12 y 24 meses para determinar el efecto del sesgo protopático. Al calcular el riesgo de cáncer, no se consideró la medicación inhalada utilizada durante el período de latencia. Se evaluó el cociente de riesgo (HR) con IC del 95 % para el riesgo de cáncer de pulmón. El análisis se realizó solo en casos con datos completos. Se consideró significativo un umbral de p < 0,05. Todos los análisis se realizaron utilizando SAS versión 9.4 (SAS Institute, Cary, NC, EE. UU.).
Declaración de Ética
El presente estudio fue aprobado por el Comité de Revisión Institucional del Hospital Universitario de Ajou (AJOUIRB-EXP-2021-582). El comité de revisión ética eximió del requisito del consentimiento informado de los pacientes estudiados.
Resultados
Características de línea base
Esta cohorte comprendió 63.442 pacientes con una edad media de 69,1 años (75,7% varones; Tabla 1). Un total de 39.588 pacientes (62,4%) fueron categorizados en el grupo LAMA/LABA, 22.718 (35,8%) en el grupo ICS/LABA y 1.136 (1,8%) en el grupo LABA (Tabla 1). La edad media del grupo ICS/LABA fue más joven y la proporción de mujeres en el grupo ICS/LABA fue mayor (p < 0,001) (Tabla 1). Entre las comorbilidades durante el período de selección, el asma fue significativamente más coexistente en el grupo ICS/LABA. La diabetes, EPID, cardiopatía isquémica, insuficiencia cardíaca y enfermedades cerebrovasculares se observaron con mayor frecuencia en el grupo LAMA/LABA (p < 0,001) (Tabla 1). En consecuencia, la puntuación del índice de comorbilidad de Charlson…