Resumen
Antecedentes
Los métodos de detección tradicionales enfrentan desafíos para satisfacer las diversas necesidades clínicas para diagnosticar cáncer de pulmón e infecciones dentro de una sola prueba. Onco-MNGS ha surgido como una solución prometedora capaz de identificar con precisión los patógenos y tumores infecciosos simultáneamente. Sin embargo, aún faltan evidencia crítica con respecto a su rendimiento diagnóstico para distinguir entre infecciones pulmonares, tumores y afecciones no tumorales no infecciosas en entornos clínicos reales.
Métodos
En este estudio, se recopilaron datos de 223 participantes que presentaron síntomas de infección pulmonar o tumor que se sometieron a pruebas de ONCO-MNGS. Los pacientes se clasificaron en cuatro grupos basados en diagnósticos clínicos: infección, tumor, tumor con infección y no infección no tumor. Se realizaron comparaciones en diferentes grupos, subtipos y etapas del cáncer de pulmón con respecto a los patrones de variación del número de copias (CNV), composiciones de microbiomas e índices de detección clínica.
Resultados
En comparación con los métodos de prueba de infección convencionales, ONCO-MNGS demuestra un rendimiento superior de detección de infecciones, con una sensibilidad del 81.82%, una especificidad del 72.55%y una precisión general del 77.58%. En el diagnóstico de cáncer de pulmón, ONCO-MNGS muestra excelentes capacidades de diagnóstico con sensibilidad, especificidad, precisión, valor predictivo positivo y valor predictivo negativo que alcanza el 88.46%, 100%, 91.41%, 100%y 90.98%, respectivamente. En muestras de fluido de lavado broncoalveolar (BALF), estos valores son de 87.5%, 100%, 94.74%, 100%y 91.67%, respectivamente. En particular, se observaron tipos de mutación de CNV más abundantes y tasas de mutación más altas en el adenocarcinoma (ADC) en comparación con el carcinoma de células escamosas (SCC). Al mismo tiempo, los datos de ONCO-MNGS revelaron un enriquecimiento específico de Capnocytophaga Sputigeria en el grupo ADC y la parapsilosis de Candida en el grupo SCC. Estas especies exhibieron correlaciones significativas con la proteína de reacción C (CRP) y los valores de CA153. Además, Haemophilus influenzae se enriqueció en el grupo SCC en etapa temprana y se asoció significativamente con los valores de CRP.
Conclusiones
ONCO-MNGS ha exhibido eficiencias excepcionales en la detección y diferenciación de la infección y el cáncer de pulmón. Este estudio proporciona una nueva opción tecnológica para lograr una detección precisa y rápida de cáncer de pulmón.
Abstracto gráfico
Introducción
El cáncer de pulmón (LC) es un tumor maligno que generalmente se origina en los tejidos pulmonares y se ubica entre las causas más importantes de las muertes relacionadas con el cáncer en todo el mundo (1). Generalmente se clasifica en dos categorías principales: cáncer de pulmón de células no pequeñas (NSCLC) y cáncer de pulmón de células pequeñas (SCLC). NSCLC abarca subtipos como adenocarcinoma (ADC), carcinoma de células escamosas (SCC) y carcinoma de células grandes (LCC) (2, 3), que constituye colectivamente aproximadamente el 85% de los casos de cáncer de pulmón (4, 5). NSCLC tiende a progresar lentamente, con síntomas tempranos que a menudo se manifiestan sutilmente, lo que hace que el diagnóstico temprano sea un desafío formidable. En contraste, SCLC exhibe un rápido crecimiento y se diagnostica típicamente después de la metástasis a otras regiones. Por lo tanto, la detección temprana y el diagnóstico preciso de cáncer de pulmón son imprescindibles para mejorar las tasas de curación y las tasas de supervivencia (6, 7).
Actualmente, en la práctica clínica, la detección de tumores generalmente implica una serie de exámenes de imágenes, que incluyen ultrasonido abdominal, radiografías de tórax y tomografías computarizadas del cofre, el abdomen y la pelvis. Estas pruebas a menudo se combinan con procedimientos invasivos como biopsias de aguja para garantizar un diagnóstico y evaluación más precisos (6). En los últimos años, los métodos innovadores como las biopsias líquidas y las pruebas de ADN tumoral circulante han mostrado un potencial significativo (7, 8), proporcionando formas más convenientes para la detección y el monitoreo temprano al tiempo que reduce las molestias y los riesgos del paciente. Los estudios han justificado la eficacia de la utilización de información derivada de humanos a partir de datos extensos de secuenciación genómica como un medio para evaluar las variaciones de número de copias (CNV) en muestras clínicas, contribuyendo así al diagnóstico y monitoreo de tumores ((11,12,13,14). Estos hallazgos indican que aprovechar la información derivada de humanos de los datos de secuenciación macro genómica es un método valioso para evaluar la CNV en muestras clínicas, contribuyendo al diagnóstico y monitoreo de tumores.
Los pacientes con cáncer de pulmón a menudo presentan síntomas clínicos que se asemejan a los de las infecciones, como la tos, la producción de esputo, el dolor en el pecho y la presencia de masas pulmonares (5, 9). La identificación y diferenciación precisas entre las infecciones y el cáncer son críticas en el diagnóstico y el tratamiento del cáncer. La identificación anterior y más rápida de los patógenos puede guiar un tratamiento antiinfeccioso individualizado preciso, lo cual es de gran importancia para controlar las infecciones pulmonares (10). La detección tradicional de infecciones se basa principalmente en métodos de cultivo, con limitaciones como bajas tasas de positividad y períodos de prueba prolongados. En los últimos años, la secuenciación metagenómica de próxima generación (MNGS) se ha convertido en una herramienta valiosa para el diagnóstico de patógenos debido a sus períodos de prueba más cortos, una cobertura de patógenos más amplia y un sesgo reducido ((11, 12). La secuenciación metagenómica permite el análisis simultáneo de los genomas del huésped y el patógeno. Sin embargo, los métodos MNGS actuales se diseñan principalmente para la rápida identificación de microorganismos patógenos relacionados con la infección y no se utilizan típicamente para la detección de tumores (13, 14).
La tecnología ONCO-MNGS recientemente desarrollada sobresale en una identificación precisa de microorganismos patógenos en muestras clínicas (15). Simultáneamente, analiza los datos del genoma humano derivados de MNG para detectar CNV dentro de los cromosomas humanos. En consecuencia, ONCO-MNGS sirve como una solución rápida de un solo paso para identificar posibles factores de infección y anomalías cromosómicas relacionadas con el tumor en líquidos corporales del paciente y muestras de tejido. Este enfoque mejora la eficiencia del diagnóstico y minimiza el impacto físico de las pruebas. En este estudio, evaluamos una cohorte clínica que comprende 233 pacientes con tumores o infecciones sospechosas utilizando ONCO-MNGS. Nuestro objetivo era investigar las capacidades de detección del cáncer de ONCO-MNGS en muestras de fluido de lavado broncoalveolar (BALF) y evaluar su eficiencia en la tipificación y estadificación del cáncer de pulmón, utilizando datos CNV y microbiológicos generados a través de ONCO-MNGS.
Métodos
Fuente de datos y diseño de estudio
Este es un estudio retrospectivo de un solo centro que analiza los datos de ONCO-MNGS y la información clínica de 223 pacientes inscritos en el Departamento de Respiratorio del primer hospital afiliado, la Universidad de Medicina de Guangzhou entre el 24 de julio de 2020 y el 2 de diciembre de 2022 (Fig. 1 y mesa 1). Solo los pacientes se sometieron a pruebas de ONCO-MNGS después de la admisión. Estos pacientes presentaron uno de los siguientes tres síntomas al ingreso: (i) una nueva aparición de tos, expectación o síntomas respiratorios empeorados, con o sin esputo purulento, dolor torácico, disnea y hemoptisis; (Ii) fiebre; (Iii) Signos de consolidación y/o rales húmedos en la auscultación pulmonar. Simultáneamente, los rayos X de tórax o los escaneos de tomografía computarizada (CT) revelaron nuevos infiltrados, consolidaciones lobernas o segmentarias, opacidades de vidrio terrestre o imágenes intersticiales. Los pacientes infectados con el virus de la inmunodeficiencia humana (VIH), los confirmados con tuberculosis al ingreso, y las mujeres embarazadas fueron excluidas. In addition to the mNGS data from BALF samples, infection-related tested results, including white blood cell (WBC), procalcitonin (PCT), C-reactive protein (CRP), neutrophil, and tumor markers such as carcinoembryonic antigen (CEA), neuron-specific enolase (NSE), cancer antigen 125 (CA125) and cancer antigen 153 (CA153), junto con otros biomarcadores obtenidos de muestras de sangre contemporánea, también se recogieron. Todos los pacientes o sus familias firmaron el formulario de consentimiento informado para la recolección y el estudio de muestras clínicas y registros médicos.
Fig. 1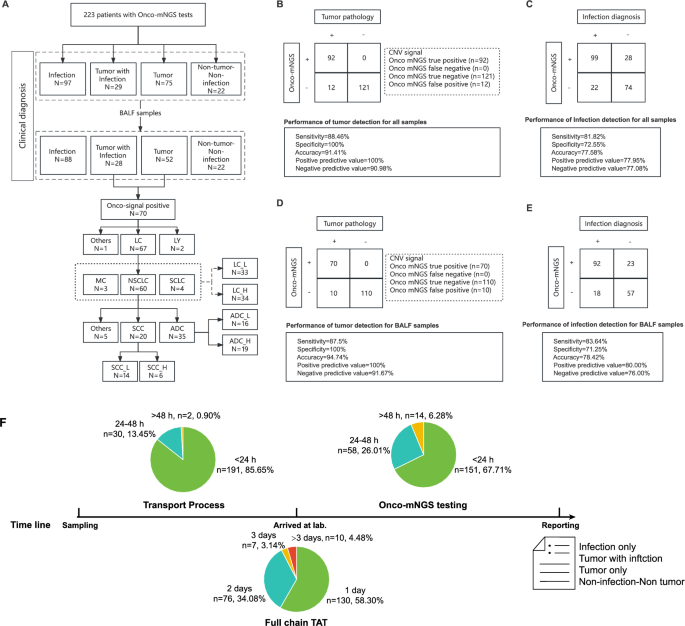
Diseño general del estudio y el rendimiento de diagnóstico de la prueba MNGS. A Diagrama de flujo de la clasificación de pacientes y muestras. Todas las muestras inscritas se analizaron utilizando Q-MNGS 2.0 y cuya clasificación se basó en diagnósticos clínicos. Todas las muestras se usaron para analizar el rendimiento de los MNG, mientras que solo las muestras BALF se incluyeron aún más para los análisis de microbiota y CNV. Muestras no tumorales y no infecciones, Cáncer de pulmón LC, linfadenoma LY, cáncer de metástasis de MC, cáncer de pulmón de células no pequeñas NSCLC, cáncer de pulmón SCLC de células pequeñas, carcinoma de células SCC SCC, Cancinoma de cáncer ADC ADC e II. (B) (D) El rendimiento de ONCO-MNGS en el diagnóstico de cánceres basados en señales de CNV en comparación con el diagnóstico clínico. (do) (mi) El rendimiento de ONCO-MNGS en el diagnóstico de infección en comparación con el diagnóstico clínico. (B) (do) incluyó todo tipo de muestras y (D) (mi) Contiene solo muestras Balf. Si los microorganismos patógenos identificados en el informe ONCO-MNGS coincidían por completo con los patógenos clínicamente confirmados como responsables, se consideró un resultado concordante. De lo contrario, el resultado de ONCO-MNGS se consideró negativo. (F) diagrama de flujo que muestra el resultado estadístico de la duración de la detección real
Imagen de tamaño completoTabla 1 Información general y resultados de laboratorio de pacientes con muestras de BALFMesa de tamaño completoExtracción de ADN, preparación y secuenciación de la biblioteca
Cada muestra se transportó a baja temperatura (bolsa de hielo) al Laboratorio de Biotecnología Guangzhou Matridx para pruebas de ONCO-MNGS. Las muestras recolectadas fueron transportadas, en una manada de hielo, al laboratorio de biotecnología Matridx para pruebas inmediatas de ONCO-MNGS. Para las muestras de líquido corporal, se usaron un total de 200 μl de líquido para la extracción de ADN. Brevemente, se utilizó un sistema de preparación de biblioteca automática NGS (Cat. Mar002, Matridx Biotech Corp., Hangzhou, China) para automatizar la extracción de ADN y la preparación de la biblioteca. Los kits acompañados fueron un kit de extracción de ácido nucleico (Cat. MD013, Matridx Biotech Corp.) y un ADN total …
(Tagstotranslate) Onco-Mngs (T) Diagnóstico de infección (T) Diagnóstico de cáncer de pulmón (T) rendimiento clínico (T) fluido de lavado bronquial (T) Sistema de neumología/respiratorio