Resumen
Antecedentes
La embolia pulmonar (EP) pone en peligro la vida y requiere un diagnóstico oportuno y preciso; sin embargo, los métodos de imagen actuales, como la angiografía pulmonar por tomografía computarizada, presentan limitaciones, particularmente para pacientes con contraindicaciones para los agentes de contraste yodados. Nuestro objetivo era desarrollar un proceso de análisis de textura cuantitativo utilizando aprendizaje automático (ML) basado en tomografías computarizadas (TC) torácicas sin contraste para descubrir características de intensidad y textura correlacionadas con la fisiología y patología de la perfusión pulmonar (Q) regional y sintetizar Q en vóxeles. sustitutos para ayudar en el diagnóstico de EP.
Métodos
Recopilamos retrospectivamente exploraciones Q-SPECT/CT con albúmina macroagregada marcada con 99mTc de pacientes con sospecha de EP, incluido un conjunto de datos internos de 76 pacientes (64 para entrenamiento, 12 para pruebas) y un conjunto de datos de pruebas externas de 49 pacientes. Las características cuantitativas de la TC se extrajeron de subregiones pulmonares segmentadas y se sometieron a un proceso de selección de características de dos etapas. La etapa de preselección basada en el conocimiento previo examinó características sólidas y no redundantes correlacionadas con la perfusión, mientras que la etapa de selección basada en datos filtró aún más las características ajustando modelos de ML para la clasificación. El modelo de clasificación final, entrenado con la combinación de características asociadas a PE de mayor rendimiento, se evaluó en las cohortes de prueba según el área bajo la curva (AUC) para la previsibilidad a nivel de subregión. Luego se sintetizó el sustituto Q vóxel utilizando los mapas de características (FM) y los mapas de puntuación del modelo (MSM) seleccionados finales para investigar las distribuciones espaciales. Se utilizaron el coeficiente de correlación de Spearman (SCC) y el coeficiente de similitud de Dice (DSC) para evaluar la consistencia espacial entre FM o MSM y las exploraciones Q-SPECT.
Resultados
El rendimiento óptimo del modelo logró un AUC de 0,863 durante las pruebas internas y de 0,828 en la cohorte de pruebas externas. El modelo identificó una combinación que contenía 14 características de intensidad y textura que no eran redundantes, robustas y capaces de distinguir entre regiones pulmonares de alta y baja funcionalidad. La evaluación de la consistencia espacial en la cohorte de pruebas internas mostró una concordancia moderada a alta entre los HSH y las exploraciones Q-SPECT de referencia, con una mediana de SCC de 0,66 y una mediana de DSC de 0,86 y 0,64 para regiones de alta y baja funcionalidad, respectivamente.
Conclusiones
Este estudio validó la viabilidad de utilizar un análisis de textura cuantitativo y un proceso de aprendizaje automático basado en datos para generar sustitutos de perfusión pulmonar por vóxeles, proporcionando una alternativa ampliamente accesible y sin radiación a las imágenes pulmonares funcionales en el tratamiento de enfermedades vasculares pulmonares.
Número de ensayo clínico
No aplicable.
Introducción
La embolia pulmonar (EP) es reconocida como la tercera causa de muerte cardiovascular, después del infarto agudo de miocardio y el accidente cerebrovascular.1). En la EP, la obstrucción de la arteria pulmonar suele ser causada por la acumulación de coágulos de sangre (trombos), burbujas de aire, tejido adiposo o líquido amniótico. Esto ocurre a menudo en personas con afecciones preexistentes, como enfermedades cardíacas, cáncer, fracturas graves o durante el embarazo (2, 3). La EP se asocia con una mortalidad significativa, particularmente en pacientes de alto riesgo que presentan shock o paro cardíaco, donde la tasa de mortalidad a 30 días puede alcanzar el 52-65%.4). Se estima que la EP afecta a entre 300.000 y 600.000 personas anualmente en los Estados Unidos, lo que provoca al menos 100.000 muertes (5, 6). Dada la etiología compleja y la rápida progresión de la EP, el diagnóstico oportuno y preciso, así como el tratamiento oportuno, son cruciales para que los médicos mejoren los resultados de los pacientes.
El diagnóstico de EP no puede basarse únicamente en la evaluación clínica, ya que los síntomas, signos y datos de laboratorio que lo respaldan a menudo son engañosamente inespecíficos.7). Aunque la angiografía pulmonar por tomografía computarizada (CTPA) es el estándar de oro para diagnosticar la EP, su uso de agentes de contraste yodados (ICA) plantea riesgos para pacientes con contraindicaciones como alergias a ICA o insuficiencia renal, lo que limita su universalidad. Los estudios han demostrado que el uso repetido de ICA aumenta el riesgo de reacciones adversas agudas (8). Según las directrices de 2019 para el diagnóstico y tratamiento de la embolia pulmonar, desarrolladas en colaboración con la Sociedad Respiratoria Europea, la tomografía computarizada por emisión de fotón único (V/Q-SPECT) de ventilación/perfusión es una de las técnicas de imagen más utilizadas en la EP. diagnóstico, con una sensibilidad y especificidad del 97% y 91%, respectivamente (9, 10). Sin embargo, la V/Q-SPECT es invasiva, costosa y menos disponible que otras modalidades de imágenes como la TC, lo que a menudo genera tiempos de espera más prolongados para las pruebas, especialmente en hospitales con recursos limitados o regiones sin instalaciones de medicina nuclear (NM).11).
Además de los exámenes convencionales de la función pulmonar basados en agentes de contraste, varios estudios han intentado obtener información de perfusión indirectamente a partir de exploraciones torácicas clínicas más comúnmente disponibles, siendo las imágenes de perfusión por tomografía computarizada (CTPI) las que reciben la mayor atención. Una categoría de técnicas CTPI emplea registro de imágenes deformables (DIR) para modelar físicamente sustitutos del suministro y circulación de sangre pulmonar a partir de exploraciones por TC relacionadas con las vías respiratorias sin contraste (es decir, TC de cuatro dimensiones, 4DCT), para restaurar la distribución de perfusión estática en el vóxel. nivel (12). Estos métodos suelen tener un proceso de modelado estricto e interpretable, pero la predicción se ve gravemente afectada por la calidad de la imagen (por ejemplo, ruido de TC y artefactos de movimiento) y los resultados de DIR. Estas limitaciones pueden provocar una variabilidad significativa en las evaluaciones de perfusión, lo que podría comprometer la precisión del diagnóstico. Además, se han propuesto algunos enfoques de aprendizaje profundo (DL) para sintetizar directamente imágenes de perfusión pulmonar a partir de una única imagen de TC a través de redes neuronales profundas.13,14,15). La aplicación de técnicas de DL de extremo a extremo, aunque innovadora y eficiente, enfrenta desafíos asociados con sus complejos procesos de toma de decisiones y la falta de consideración de mecanismos patológicos clínicamente relevantes. En general, aunque todavía se encuentra en las primeras etapas de desarrollo, la aparición de CTPI tiene el potencial de reducir el uso indebido de agentes de contraste y mejorar la eficiencia de los técnicos clínicos.
Para abordar estos desafíos, este estudio amplía las exploraciones CTPI aprovechando las capacidades del análisis cuantitativo de textura. El análisis de textura es capaz de extraer características de alta dimensión de imágenes de TC sin contraste de rutina que normalmente no son discernibles para el ojo humano. Estas características luego se pueden transformar cuantitativamente en biomarcadores de imágenes con definiciones matemáticas explícitas (16, 17). Al centrarse en la extracción y la interpretabilidad de características, nuestro enfoque mitiga los problemas de «caja negra» que se observan en los métodos DL, al mismo tiempo que aborda las limitaciones de la calidad de la imagen mediante una sólida selección de características y optimización del modelo. Nuestro objetivo fue realizar el análisis de textura cuantitativo y el proceso de aprendizaje automático (ML) basado en datos en tomografías computarizadas torácicas sin contraste para descubrir características de intensidad y textura que se correlacionan con la fisiología y patología de la perfusión pulmonar regional subyacente. Además, al estudiar la distribución espacial de las características correlacionadas con la perfusión y los resultados del modelo ajustado, desarrollaremos un método confiable e interpretable para predecir sustitutos de perfusión pulmonar por vóxeles. El método propuesto representa una perspectiva novedosa sobre CTPI y ofrece una referencia diagnóstica potencialmente mejorada sobre EP y otras enfermedades pulmonares relacionadas con la perfusión.
Materiales y métodos
Descripción general del flujo de trabajo
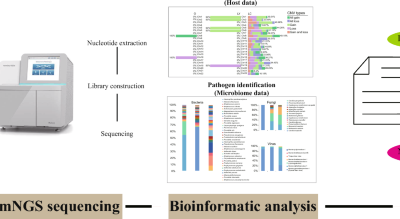
Cifra 1 Representa el flujo de trabajo general de este estudio. En la etapa de selección de características, las regiones pulmonares en las imágenes de TC de todos los pacientes se segmentaron en múltiples subregiones. Según un umbral específico del sujeto, cada subregión pulmonar de TC se etiquetó binariamente como de alto o bajo funcionamiento según su señal Q-SPECT promediada espacialmente. Dentro de cada subregión funcional alta o baja, se extrajeron características para obtener información de intensidad y textura y se sometieron a un proceso de selección de características de dos etapas. La etapa de preselección basada en el conocimiento previo inicialmente examinó características correlacionadas con perfusión sólidas y no redundantes, mientras que la etapa de selección basada en datos filtró aún más las características ajustando modelos de ML para una tarea de clasificación. El modelo de clasificación final se entrenó con la combinación de características asociadas a PE de mayor rendimiento y se evaluó para determinar la previsibilidad a nivel de subregión. Se generaron mapas de características (FM) y mapas de puntuación de modelos (MSM) de las características finales seleccionadas para estudiar sus distribuciones espaciales y como posibles mapas de perfusión sustitutos. El coeficiente de correlación de Spearman (SCC) en términos de vóxeles y el coeficiente de similitud de Dice (DSC) para los volúmenes pulmonares funcionales se utilizaron para evaluar la consistencia espacial entre FM o MSM y las exploraciones Q-SPECT. Las etapas clave de este flujo de trabajo se especifican con más detalle a continuación.
Figura 1El flujo de trabajo general del estudio.
Imagen a tamaño completoDatos del paciente y preprocesamiento
El conjunto de datos de descubrimiento interno se recopiló retrospectivamente de una base de datos utilizada previamente en nuestra investigación (14), con la aprobación de la Junta de Revisión Institucional (IRB) de la institución afiliada. La base de datos sin procesar incluye 173 pacientes que se sometieron a una exploración Q-SPECT/TC con albúmina macroagregada marcada con 99mTc (99mTc-MAA) pulmonar en el Queen Mary Hospital, de 2019 a 2023 por sospecha de enfermedades pulmonares. Las características de los pacientes se resumen en el Apéndice A. Los criterios de exclusión de sujetos para este estudio consistieron en otras afecciones pulmonares, como hipertensión pulmonar, cáncer de pulmón o insuficiencia cardíaca congestiva, así como imágenes pulmonares incompletas. Además, se incluyó un conjunto de datos de pruebas externas de exploraciones Q-SPECT/CT recopiladas entre 2020 y 2023 en el Tercer Hospital de la Universidad de Pekín (Fig. 2) y fue aprobado por el Comité de Ética en Investigación en Ciencias Médicas de la institución afiliada.
Figura 2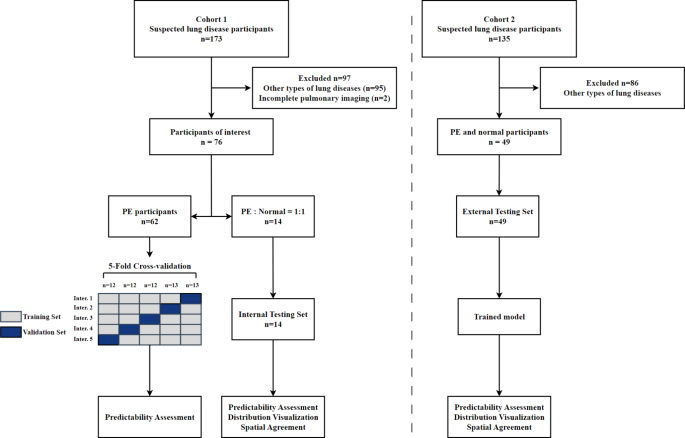
El diagrama de flujo de las exploraciones Q-SPECT/CT incluidas en el…