Resumen
Antecedentes
La embolia pulmonar aguda (APE) es una enfermedad crítica con una alta tasa de mortalidad, algunos de los pacientes sobrevivientes pueden desarrollar enfermedad pulmonar tromboembólica crónica (CTEPD), lo que afecta el pronóstico del paciente. Sin embargo, la investigación sobre el diagnóstico temprano de CTEPD es limitada. Este estudio tuvo como objetivo establecer un modelo de predicción para la identificación anterior de CTEPD.
Métodos
Este estudio prospectivo incluyó 464 pacientes consecutivos con APE confirmado entre enero de 2020 y septiembre de 2023, en 7 centros de China. Después del seguimiento durante al menos 3 meses, los pacientes se dividieron en los grupos CTEPD y no PTEPD en función de los síntomas y la tomografía computarizada de la angiografía pulmonar (CTPA) o las exploraciones de perfusión de ventilación pulmonar (V/Q) que muestran trombosis residual. Los factores de riesgo independientes para CTEPD se identificaron a través de análisis de regresión logística univariados y multivariados. A continuación, se estableció un nomograma de modelo predictivo, y la validación se completó mediante análisis de curva de decisión (DCA) y análisis de curva de características operativas del receptor.
Resultado
En total, 130 (28%) pacientes presentaron CTEPD, 17% (22/130) de pacientes con CTEPD desarrollaron hipertensión pulmonar tromboembólica crónica (CTEPH). Basado en el análisis multivariado, un intervalo de tiempo desde el inicio de los síntomas hasta el diagnóstico (tiempo de diagnóstico) ≥ 15 días (intervalo de confianza (IC) del 95%: 3.392–14.972, p <0.001), embolismo pulmonar recurrente (RPE) (95 (95) (95 %De IC: 1.560–17.300, p = 0.007), disfunción ventricular derecha (RVD) (IC 95%: 1.042–6.437, p = 0.040), émocolos centrales (IC 95%: 1.776–7.383, p <0.001) y pulmonario residual residual La obstrucción vascular (RPVO)> 10% (IC 95%: 4.884–21.449, p <0.001) se identificaron como los predictores independientes de CTEPD. Luego, se estableció un modelo de predicción con un índice C de 0.895 (IC 95% 0.863–0.927) para pacientes de alto riesgo. El nomograma tuvo un excelente rendimiento predictivo para la identificación anterior de CTEPD, con un área bajo la curva de 0.908 (IC 95%: 0.875–0.941) en la cohorte de entrenamiento y 0.875 (IC 95%: 0.803–0.947) en la cohorte de validación.
Conclusión
El estudio actual estableció y validó un nomograma confiable para predecir CTEPD, lo que ayudaría a los médicos a identificar a los pacientes de alto riesgo para CTEPD anteriormente.
Introducción
La embolia pulmonar aguda (APE) es un grupo de síndromes clínicos causados por embolia endógena o exógena que bloquea la arteria pulmonar (PA) o sus ramas (1). Se asocia con una mortalidad y morbilidad significativas y es la tercera causa más común de mortalidad por cardiovascular después del infarto y el accidente cerebrovascular (accidente cerebrovasculares (2). Anstoagulación, y la reperfusión de la AP son los principales tratamientos para APE (3).
Con los avances significativos en las estrategias de tratamiento, la mortalidad general a corto plazo de los pacientes con APE ha disminuido. Sin embargo, hasta el 50% de los pacientes presentan defectos de perfusión persistentes después de un simio (4, 5). Todos los pacientes con síntomas que pueden atribuirse a las obstrucciones fibróticas posifrombólicas dentro de la AP tienen enfermedad pulmonar tromboembólica crónica (CTEPD), que puede acompañarse de hipertensión pulmonar en reposo (pH) (PH) (6,7,8). CTEPD es una entidad de la enfermedad que pertenece a un grupo más amplio de enfermedades que afectan la vasculatura arterial pulmonar causada por la embolia pulmonar (PE). Además, es una enfermedad progresiva, potencialmente mortal e irreversible (9). Las manifestaciones clínicas de CTEPD no son específicas. Por lo tanto, la condición a menudo se diagnostica o se pierde erróneamente. Los estudios actuales se han centrado comúnmente en la progresión y los factores de riesgo de APE, y la investigación sobre la detección temprana y oportuna de CTEPD es limitada (10,11,12). Por lo tanto, una herramienta simple y efectiva que puede usarse para evaluar el riesgo individualizado y la progresión de CTEPD deben desarrollarse con urgencia para facilitar la intervención temprana.
El estudio actual tuvo como objetivo analizar los factores de riesgo asociados con CTEPD durante el seguimiento en pacientes con APE utilizando un modelo de predicción clínica para la identificación temprana de pacientes de alto riesgo.
Métodos
Participantes
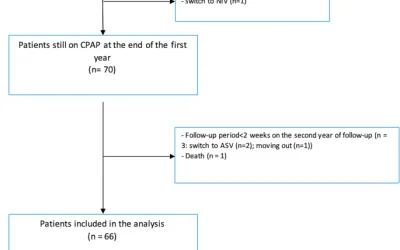
Los pacientes consecutivos con APE confirmados entre enero de 2020 y septiembre de 2023, en 7 centros de China, fueron reclutados prospectivamente. Los criterios de inclusión fueron los siguientes: (1) Todos los pacientes que fueron diagnosticados con APE en tomografía computarizada angiografía pulmonar (CTPA) o exploración de perfusión de ventilación pulmonar (V/Q) (13); (2) aquellos de edad> 18 años; (3) y aquellos con imágenes completas y datos clínicos y consentimiento informado. Los criterios de exclusión fueron los siguientes: (1) pacientes con embolia pulmonar crónica; (2) aquellos con defecto de llenado de PA debido a la vasculitis y otras razones; (3) y aquellos que suspendieron el tratamiento con anticoagulantes en 3 meses y que fueron pérdidas por el seguimiento (14). Cifra 1 muestra el diagrama de flujo de la selección de participantes.
Fig. 1Los participantes seleccionaron el diagrama de flujo
Imagen de tamaño completoEste estudio se realizó de acuerdo con la Declaración de Helsinki (revisado en 2013) y fue aprobado por los comités de ética del Hospital Provincial Shandong (SWYX: No. 2019-070). Todos los pacientes proporcionaron consentimientos informados.
Recopilación de datos
Datos sobre características demográficas, síntomas, condiciones de comorbilidades, factores de riesgo, prueba de laboratorio, electrocardiograma, ecocardiografía transtorácica (TTE), ultrasonografía Doppler de extremidades inferiores, se registraron resultados de exploración CTPA y V/Q. Todos los pacientes se inscribieron con parámetros TTE, y PE fue diagnosticado por CTPA o escaneo V/Q. Las imágenes son interpretadas parcialmente por 2 especialistas experimentados.
Criterios de CTEPD: pacientes con APE que recibieron terapia anticoagulante adecuada durante al menos 3 meses y aquellos que presentaron síntomas similares como disnea, defectos de perfusión y obstrucciones fibróticas organizadas en pacientes con o sin pH en reposo (6). En este estudio, de acuerdo con las pautas de 2022 ESC/ERS para el diagnóstico y el tratamiento de la hipertensión pulmonar, el diagnóstico de CTEPD se consideró para todos los pacientes con APE que exhibieron síntomas después de al menos 3 meses de anticoagulación regular, y tuvieron una trombosis residual confirmada por CTPA por CTPA. o V/Q Scan.
Visualización de la disfunción ventricular del ventrículo derecho (RVD) en TTE: ventricular derecha dilatada (RV) con RV basal/ventrículo izquierdo (LV)> 1.0, hipocinesis de la pared libre ventricular libre o movimiento anormal anormal del tabique intervencicular, gradiente sistólico pico en el tricuspid válvula> 30 mmHg, y tricúspide excursión sistólica del plano anular (TAPSE) <16 mm (13, 15, 16).
La obstrucción vascular pulmonar residual (RPVO) se define como una repermeabilización incompleta de las arterias pulmonares después de APE (4). La gravedad anatómica de RPVO se cuantificó de acuerdo con el puntaje Qanadli y Meyer (17, 18).
Todos los pacientes se dividieron aleatoriamente en las cohortes de entrenamiento y validación en una relación 7: 3 usando R con RStudio.
Resultados primarios
Los pacientes fueron seguidos durante al menos 3 meses a través de visitas al hospital o entrevista telefónica, y los resultados primarios fueron sobre el diagnóstico de CTEPD.
Análisis estadístico
Los datos se analizaron utilizando el paquete estadístico para el software de ciencias sociales (versión 25.0, IBM Inc, Chicago, IL, EE. UU.). Las variables continuas tenían una distribución normal y se expresaron como media ± desviación estándar (DE). Mientras tanto, las variables categóricas se expresaron como frecuencia y porcentajes. La prueba t se utilizó para comparar las variables continuas con los resultados de la investigación, y la prueba 𝜒2 se utilizó para comparar las variables categorizadas.
Se utilizaron análisis univariados y multivariados utilizando modelos de regresión logística para probar la importancia de los factores de riesgo independientes. Las variables con valores de P de <0.05 en el análisis univariado se ingresaron en el análisis multivariado para estimar la importancia de cada variable. Se estableció un nomograma para predecir CTEPD en base a los predictores independientes, que se construyeron utilizando R (versión 4.3.2; R Foundation for Statistical Computing) con RStudio (versión 2023.12.0; RStudio). El rendimiento del nomograma para discriminar y calibrar se midió en la cohorte de entrenamiento utilizando el índice de concordancia Harrell (índice C), el área bajo la curva (AUC) de la curva característica operativa del receptor (ROC), gráficos de calibración y análisis de curva de decisión (DCA). Luego, el nomograma fue validado en la cohorte de validación. Los valores de P de <0.05 se consideraron significativos.
Resultados
Características basales de los pacientes
En total, se incluyeron 464 pacientes con APE en este estudio, y 70 (53.85%) pacientes eran mujeres. Las edades promedio de los grupos CTEPD y no TTEPD fueron 61.71 (DE ± 14.24) y 64.39 (DE ± 13.85) años, respectivamente. Datos sobre las características básicas enumeradas en la tabla 1 se obtuvieron de los registros médicos electrónicos del hospital. La mediana del tiempo de seguimiento fue de 12 (rango intercuartil: 3–24) meses. La incidencia general de CTEPD fue del 28%, 17% (22/130) de pacientes con CTEPD desarrolló hipertensión pulmonar tromboembólica crónica (CTEPH). Cifra 2 muestra la incidencia acumulada de CTEPD. Disnea, dolor en el pecho, intervalo de tiempo desde el inicio de los síntomas hasta el diagnóstico (tiempo de diagnóstico) ≥ 15 días, EP recurrente (RPE), cáncer, enfermedades del tejido conectivo (CTD), RVD, embolia central, RPVO> 10%, estratificación de riesgo y la puntuación simplificada del índice de gravedad de la embolia pulmonar (SPESI) era importante indicadores clínicos importantes de CTEPD (todos los valores de P <0.05). Los indicadores restantes no difirieron significativamente.
Tabla 1 Características basales en pacientes de APEMesa de tamaño completoFig. 2
Incidencia acumulada de CTEPD en 464 pacientes seguidos después de APE
Imagen de tamaño completoSelección de factores de riesgo clínico
Mesa 2 Muestra los datos clínicos de los pacientes en la cohorte de entrenamiento (n = 324) y la cohorte de validación (n = 140). Los predictores independientes de CTEPD se seleccionaron en base a análisis univariados y multivariados, como se muestra en la tabla 3. Disnea, dolor en el pecho, tiempo de diagnóstico ≥ 15 días, RPE, cáncer, CTD, …
(Tagstotranslate) Embolismo pulmonar agudo (T) Factores de riesgo (T) Enfermedad tromboembólica crombólica (T) Modelo de predicción (T) Sistema de neumología/respiratorio Sistema respiratorio