Resumen
Antecedentes
La fibrosis pulmonar idiopática (FPI) es una enfermedad pulmonar compleja con muy mal pronóstico. Los fármacos existentes para el tratamiento de la FPI siguen siendo insuficientes. Por lo tanto, todavía es necesario explorar nuevos objetivos farmacológicos para prevenir y tratar la FPI.
Métodos
Incluimos loci de rasgos cuantitativos (QTL) para genes, metilación del ADN y proteínas en plasma, así como el resumen estadístico de FPI. Se utilizaron como variables instrumentales variantes genéticas ubicadas dentro de 500 kb del gen y fuertemente asociadas con la exposición al plasma. La asociación causal entre las exposiciones al plasma y la FPI se estimó principalmente mediante un análisis de aleatorización mendeliana (SMR) basado en datos resumidos. Se emplearon otros cinco métodos de RM y análisis de sensibilidad para validar los resultados de la RME. Las pruebas bayesianas de colocalización entre los loci de riesgo QTL e IPF fortalecen aún más los resultados de la RM.
Resultados
Identificamos tres genes y cinco sitios de metilación del ADN causalmente asociados con la FPI mediante análisis SMR, validación del análisis MR, análisis de sensibilidad y análisis de colocalización. BTRC y LINC01252 se asociaron negativamente con el riesgo de FPI (OR: 0,30, IC del 95 %: 0,17–0,54, FDRSMR = 0,029; OR: 0,85, IC del 95 %: 0,78–0,92, FDRSMR = 0,043), y RIPK4 se asoció positivamente con la FPI riesgo (OR: 2,60, IC 95%: 1,64–4,12, FDRSMR = 0,031). cg00045227 (OR8U8, OR: 1,16, IC del 95 %: 1,08–1,24, FDRSMR = 0,010), cg00577578 (GBAP1, OR: 1,23, IC del 95 %: 1,12–1,36, FDRSMR = 0,014), cg14222479 (ARPM1, OR: 3,17, IC del 95 %: 1,98–5,08, FDRSMR = 0,001) y cg19263494 (PMF1, OR: 1,20, IC del 95 %: 1,10–1,30, FDRSMR = 0,012) se asociaron positivamente con el riesgo de FPI, mientras que cg07163735 (MAPT, OR: 0,22; IC del 95 %: 0,11–0,45, FDRSMR = 0,013) se correlacionó negativamente con el riesgo de FPI.
Conclusiones
Este estudio demostró que los niveles plasmáticos determinados genéticamente de los genes BTRC, RIPK4 y LINC01252, así como los niveles de metilación de cg00045227 (OR8U8), cg00577578 (GBAP1), cg07163735 (MAPT), cg14222479 (ARPM1) y cg19263494 (PMF1), tener influencias causales sobre el riesgo de FPI.
Fondo
La fibrosis pulmonar idiopática (FPI) es una enfermedad pulmonar intersticial crónica, rara e irreversible caracterizada por disnea y deterioro progresivo de la función pulmonar. El pronóstico de la FPI es malo, con una esperanza de vida promedio de 3 a 5 años después del diagnóstico sin tratamiento.1,2,3). En las poblaciones de América del Norte y Europa, la incidencia de casos varía de 3 a 9 por 100.000 personas por año, y esta incidencia general tiende a aumentar con el tiempo (4). Además, a medida que la población mundial envejece, se espera que la FPI tenga un impacto significativo en la carga de salud pública mundial (5). El mecanismo de la fibrosis en la FPI aún no se conoce bien. Se cree ampliamente que la FPI es causada por microlesiones repetidas al epitelio pulmonar envejecido y disfuncional. Esto conduce a una comunicación anormal entre las células epiteliales y mesenquimales, lo que resulta en un desequilibrio entre los mediadores profibróticos y antifibróticos. En última instancia, esto conduce a que la fibrosis crónica reemplace los mecanismos de reparación normales (6, 7).
Actualmente, la clave para el tratamiento de la FPI es frenar la progresión de la enfermedad. Las guías de práctica clínica más recientes recomiendan sólo dos fármacos para el tratamiento de la FPI: pirfenidona y nintedanib.8). La pirfenidona puede inhibir eficazmente la respuesta fibrótica inducida por TGF-β, pero sus otros mecanismos para ralentizar la progresión de la FPI siguen sin estar claros.9). Nintedanib es un potente inhibidor de los receptores FGF, PDGF y VEGF, y estudios previos han encontrado que nintedanib tiene actividad inhibidora de la señalización en fibroblastos y miofibroblastos.10). Se han probado varios otros fármacos en estudios para el tratamiento de la FPI, como la pentraxina 2 humana recombinante, pamrevlumab, treprostinil inhalado y N-acetilcisteína.8). De estos, los estudios de FPI con pentraxina 2 humana recombinante y pamrevlumab se cancelaron debido a la improbabilidad de cumplir o no cumplir el criterio de valoración principal. Se están utilizando treprostinil y N-acetilcisteína inhalados para realizar estudios clínicos de FPI. En resumen, los tratamientos actuales para la FPI siguen siendo insatisfactorios. Por lo tanto, la identificación temprana de personas en riesgo de FPI y el desarrollo de nuevas intervenciones terapéuticas para reducir la alta tasa de mortalidad asociada con la FPI son cruciales.
Las exposiciones ambientales y la predisposición genética son los dos focos principales de investigación sobre la patogénesis de la FPI. Los biomarcadores genéticos pueden identificar a los pacientes con mayor riesgo de desarrollar fibrosis pulmonar y predecir la progresión de la enfermedad. Actualmente, las variantes genéticas comunes asociadas con la FPI son las variantes MUC5B y DSP, que se cree que tienen una asociación significativa con el riesgo de desarrollar FPI.11,12,13).
Recientemente, el análisis de aleatorización mendeliana (MR) se ha utilizado ampliamente para estudiar asociaciones causales e identificar posibles objetivos farmacológicos.14). La RM utiliza polimorfismos de un solo nucleótido (SNP) como herramienta genética para estimar el efecto causal de una exposición sobre un resultado. La RM evita el sesgo de factores de confusión no observados, así como la causalidad inversa (15, 16). La RM basada en datos resumidos (SMR) utiliza estadísticas resumidas independientes del estudio de asociación de todo el genoma de la enfermedad (GWAS) y datos del locus de rasgos cuantitativos (QTL) para identificar posibles genes causantes de una enfermedad (17). Sin embargo, hasta la fecha, ningún estudio de RM ha integrado datos de expresión génica plasmática QTL (eQTL), metilación del ADN QTL (mQTL) y expresión de proteínas QTL (pQTL) para investigar posibles factores genéticos causantes de la FPI. Por lo tanto, el presente estudio fue diseñado para examinar los efectos causales del gen plasmático, la metilación del ADN y el nivel de proteína en la FPI mediante análisis de resonancia magnética.
En el presente estudio, realizamos análisis SMR y HEIDI basados principalmente en datos de eQTL, mQTL y pQTL en plasma. En segundo lugar, los principales hallazgos se validaron adicionalmente mediante análisis de resonancia magnética (paquete TwoSampleMR R), análisis de sensibilidad y análisis de colocalización. Además, validamos las variantes genéticas comunes asociadas con la FPI utilizando datos eQTL del tejido pulmonar.
Métodos
Este estudio se llevó a cabo de acuerdo con las pautas de Fortalecimiento de la presentación de informes de estudios observacionales en epidemiología mediante resonancia magnética (Tabla T1).
Diseño del estudio y fuente de datos.
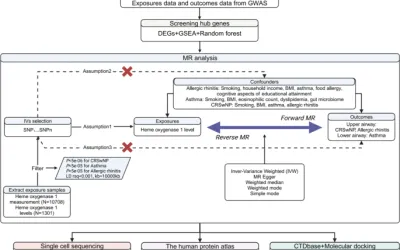
El diseño del estudio y el flujo de trabajo de este estudio se muestran en la Fig. 1. Nuestro análisis constó de dos partes. En la primera etapa, evaluamos la expresión de genes plasmáticos, la metilación del ADN y la expresión de proteínas para determinar la causalidad contra la FPI utilizando métodos de análisis SMR. En la segunda etapa, se realizó el análisis MR (paquete TwoSampleMR R) para validación y análisis de sensibilidad. Además, realizamos el análisis de colocalización.
Figura 1El diseño del estudio y el flujo de trabajo.
Imagen a tamaño completoLas estadísticas resumidas cis-eQTL se derivan del Consorcio QTLGen, que proporciona información sobre 10,317 SNP asociados con rasgos de 31,684 individuos (18). Extrajimos variantes genéticas ubicadas dentro de una ventana de 500 kb de la secuencia codificante de los datos resumidos de eQTL. Es más probable que estas variantes tengan un efecto específico sobre el gen diana. Sin embargo, eQTLGen carece de información genética sobre los cromosomas sexuales y sobre el ADN mitocondrial. Los datos resumidos de mQTL se obtuvieron de un metanálisis de datos de metilación del ADN en sangre periférica de dos cohortes (n = 1980) (19). El estudio incluyó SNP dentro de una ventana de 500 Kb para cada sonda. Las estadísticas resumidas para pQTL incluyeron 4.435 proteínas plasmáticas de 7.213 estadounidenses de origen europeo (20). Extrajimos cis-SNP dentro de una ventana de 500 Kb de genes codificadores de proteínas que están estrechamente asociados con la expresión de proteínas. Las estadísticas resumidas de IPF se obtuvieron de la última versión de la base de datos FinnGen (21). La cohorte contiene 2.018 casos y 373.064 controles. Todas las fuentes de datos están disponibles en la tabla T2.
Todas las estadísticas resumidas de GWAS se alinearon con la secuencia de referencia GRCh37. Los datos GWAS que utilizaron GRCh38 como secuencia de referencia se convirtieron utilizando el software CrossMap para garantizar la alineación con la secuencia de referencia GRCh37 (22).
Análisis estadístico
Análisis SMR
El análisis de RM se basa en tres supuestos básicos. Supuesto 1: Las variables instrumentales (VI) están fuertemente correlacionadas con la exposición. Supuesto 2: Los IV son independientes de los factores de confusión. Supuesto 3: Los IV afectan el resultado únicamente a través de la exposición. Aquí, realizamos el análisis SMR desde la línea de comandos usando la versión 1.3.1 del software SMR para sistemas Windows (https://yanglab.westlake.edu.cn/software/smr/#Overview) (17). SMR emplea un método de mínimos cuadrados de dos pasos (2SLS) para la estimación causal, utilizando variantes genéticas que están significativamente asociadas con la exposición como IV.
Este estudio utilizó el umbral P <5e-8 para seleccionar el QTL asociado para la prueba SMR. En la prueba de heterogeneidad en instrumentos dependientes (HEIDI), para cada sonda, el análisis solo incluirá SNP con valores QTL P <1,57e-03, luego excluirá los SNP con desequilibrio de ligamiento (LD) r-cuadrado con SNP superior > 0,90 o < 0,05. La fórmula de causalidad es:
$${{rm{beta }}_{{rm{exposición – FPI}}}}{rm{ = }}{{rm{beta }}_{{rm{SNP – FPI} }}}{rm{/ }}{{rm{beta }}_{{rm{SNP – exposición}}}}$$Exposición β: la FPI cuenta el tamaño del efecto estimado de los niveles de exposición plasmática (gen, metilación del ADN o proteína) en la FPI. La exposición a βSNP es el tamaño del efecto de los SNP en la exposición al plasma. βSNP-IPF representa el tamaño del efecto de los SNP en la FPI. Las estimaciones del odds ratio (OR) de la exposición al plasma sobre el riesgo de FPI se calcularon mediante ORexposición-FPI = exp (exposición β-FPI), siendo exp la base del logaritmo natural.
Utilizamos el método Benjamini-Hochberg para controlar la tasa de descubrimiento falso (FDR) de múltiples pruebas. Las asociaciones con valores de p ajustados de Benjamini-Hochberg inferiores a 0,05 se consideraron significativas. También realizamos una prueba HEIDI utilizando SMR para detectar el efecto del enlace. Una prueba HEIDI con un nivel de significancia de P < 0,01 sugiere que la asociación observada puede deberse a...