Resumen
Fondo
La embolización de la arteria bronquial (BAE) es una opción de tratamiento eficaz para controlar la hemoptisis en el cáncer de pulmón primario. Sin embargo, ningún estudio ha investigado el material de embolización óptimo para BAE en pacientes con cáncer de pulmón. Por lo tanto, este estudio tuvo como objetivo comparar la seguridad y la eficacia de la BAE realizada con norte-butil-2-cianoacrilato (NBCA) y partículas de alcohol polivinílico (PVA) en pacientes con cáncer de pulmón primario para determinar qué material embólico es mejor para pacientes con hemoptisis.
Métodos
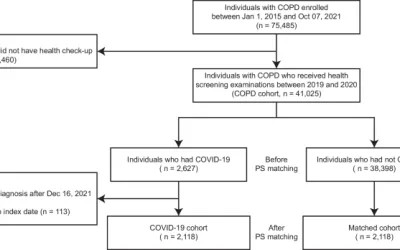
Este estudio retrospectivo fue aprobado por la junta de revisión institucional y se renunció al consentimiento. Las tasas de hemostasia, complicaciones, tiempo del procedimiento, producto dosis-área y supervivencia libre de hemoptisis se compararon retrospectivamente entre el cáncer de pulmón primario (cáncer de células no pequeñas [n = 111] y celda pequeña [n = 11]) pacientes que se sometieron a BAE con NBCA (n = 58) o partículas de PVA (n = 64) entre enero de 2004 y diciembre de 2019. Los predictores de hemoptisis recurrente se analizaron mediante el modelo de regresión de riesgos proporcionales de Cox.
Resultados
Entre 122 pacientes (edad media, 66 ± 10 años; rango 32–86 años; 103 hombres), más pacientes en el grupo NBCA (81,0 %; 47 de 58) lograron hemostasia completa que los pacientes en el grupo PVA (53,1 %; 34 de 64) (PAGS= 0,002). No se observaron complicaciones mayores en ninguno de los grupos. El tiempo del procedimiento (36,4 ± 21,6 vs. 56,3 ± 27,4 min, PAGS< 0,001) fue más breve y el producto dosis-área (58,6 ± 64,0 vs. 233,5 ± 225,0 Gy*cm2, PAGS< 0,001) fue menor en el grupo NBCA que en el grupo PVA. La mediana de supervivencia libre de hemoptisis fue de 173,0 en el grupo NBCA en comparación con 20,0 días en el grupo PVA (PAGS< 0,001). El uso de PVA (PAGS< 0,001) y coagulopatía (PAGS= 0,014) fueron predictores independientes de supervivencia libre de hemoptisis acortada.
Conclusión
La BAE con NBCA mostró una hemostasia inicial significativamente superior con una supervivencia libre de hemoptisis más larga, un tiempo de procedimiento más corto y una dosis de radiación reducida que la BAE con partículas de PVA. El uso de APV y la coagulopatía fueron predictores independientes de hemoptisis recurrente.
Registro de prueba: Registrado retrospectivamente
Fondo
La embolización de las arterias bronquiales (BAE) es un tratamiento seguro y eficaz para la hemoptisis [1,2,3,4,5,6,7,8,9]. La mayoría de las investigaciones anteriores se han centrado en la utilidad de BAE para enfermedades benignas, como bronquiectasias, tuberculosis y aspergilosis. [1,2,3, 7, 8]. Según la literatura, hasta el 30 % de los pacientes con cáncer de pulmón primario desarrollan hemoptisis, y el 10 % experimenta hemoptisis masiva [4, 5]. Unos pocos estudios sobre BAE para la hemoptisis debida a una enfermedad maligna informaron una tasa de éxito clínico relativamente baja en comparación con aquellos con enfermedad benigna. [4,5,6, 10, 11]. Sin embargo, estos están limitados por una pequeña población de estudio. [4]entidad patológica heterogénea que abarca neoplasia maligna primaria a secundaria [5, 10,11,12]y falta de uso estandarizado de materiales embólicos [4, 5, 10,11,12].
Los agentes embólicos particulados como el alcohol polivinílico (PVA), las partículas de esponja de gelatina absorbible y las microesferas de tris-acilo se han utilizado ampliamente para la BAE. Los resultados clínicos entre los pacientes sometidos a embolización con diferentes partículas son similares [2, 13]; sin embargo, no hay evidencia ni consenso en cuanto al material embólico [1, 2, 7].
El interés en que BAE utilice norte-butil-2-cianoacrilato (NBCA) ha aumentado recientemente, debido a varias ventajas que ofrece este agente; estos incluyen la embolización rápida y permanente de los vasos, tasas de polimerización controlables (ajustando la proporción de NBCA a aceite yodado) y un tiempo de procedimiento relativamente corto [1, 3, 7, 9]. Yoo et al. [1] mostró que el uso de NBCA en BAE fue factible y efectivo en 108 pacientes con enfermedades benignas. Woo et al. [7] también mostró que NBCA era un mejor material embólico que las partículas de PVA para prevenir la hemoptisis recurrente. Sin embargo, hasta donde sabemos, ningún estudio se ha centrado en BAE realizado con NBCA para controlar la hemoptisis en pacientes con cáncer de pulmón primario. Por lo tanto, este estudio tuvo como objetivo comparar retrospectivamente la seguridad y eficacia de BAE usando NBCA y partículas de PVA en pacientes con cáncer de pulmón primario y determinar qué material embólico (NBCA o partículas de PVA) es mejor para pacientes con hemoptisis.
materiales y métodos
Pacientes
La junta de revisión institucional del Hospital Bundang de la Universidad Nacional de Seúl aprobó este estudio retrospectivo (B-2008-631-111). Se eliminó el requisito de consentimiento informado. Las características basales de ambos grupos se muestran en la Tabla 1. Este estudio incluyó pacientes con cáncer de pulmón primario que se sometieron a BAE entre marzo de 2004 y diciembre de 2019. El cáncer de pulmón primario se diagnosticó mediante biopsia percutánea o broncoscópica, y la estadificación se determinó mediante tomografía computarizada (TC) de tórax, tomografía por emisión de posición y gammagrafía ósea. Los criterios de exclusión fueron los siguientes: historia previa de BAE antes del diagnóstico de cáncer de pulmón; BAE tras tratamiento curativo de cáncer de pulmón sin enfermedad residual; otros cánceres concomitantes, incumplimiento del seguimiento dentro de 1 mes después de BAE; causa poco clara de hemoptisis debido a bronquiectasias, tuberculosis o aspergiloma concomitantes; datos faltantes de la historia clínica electrónica; y sangrado post-biopsia. Se realizó una búsqueda computarizada de registros médicos electrónicos basada en palabras clave para obtener datos relacionados con la demografía, el cáncer y la hemoptisis de los grupos NBCA y PVA; los pacientes fueron seleccionados consecutivamente.
Trámites BAE
Todos los procedimientos BAE fueron realizados por uno de los cuatro radiólogos intervencionistas (JHL, CJY, HCK y HJJ). El tipo de agentes embólicos (PVA o NBCA) se seleccionó aleatoriamente a criterio de los radiólogos intervencionistas asistentes. Ambos agentes embólicos se utilizaron de forma rutinaria durante el estudio sin pausa ni período de transición. Después de obtener un acceso a la arteria femoral derecha o izquierda con una vaina vascular 5-F, se realizó una aortografía torácica utilizando un catéter pigtail 5-F (Royal Flush®; Cook Medical, Bloomington, IN, EE. UU.) con la punta colocada en la parte ascendente. aorta. La angiografía selectiva de las arterias colaterales sistémicas bronquiales y no bronquiales se realizó utilizando catéteres angiográficos de forma 5-F (GRB, Cobra, Headhunter; Cook Medical). Los siguientes hallazgos angiográficos se consideraron patológicos: rubor tumoral, arterias tortuosas que alimentan el tumor y cortocircuito broncopulmonar [6, 7]. Todas las arterias sistémicas bronquiales y no bronquiales patológicas fueron embolizadas. Se introdujo coaxialmente un microcatéter de 2 o 3 F (Progreat, Terumo, Tokio, Japón; Microferret, Cook Medical; Renegade, Boston Scientific, Natick, MA, EE. UU.) y se avanzó lo más distalmente posible para evitar el reflujo de agentes embólicos. en las arterias espinales o la aorta.
En el grupo de PVA, se diluyeron partículas de PVA de 355–500 μm (partículas de embolización de PVA Contour, Boston Scientific; partículas de embolización de espuma de PVA, Cook Medical) con 5 ml de solución salina y 15 ml de contraste en una jeringa de 20 ml conectada a un 1 Jeringa de administración de ml a través de una llave de paso de tres vías [2, 6, 7]. El criterio de valoración de la embolización fue el cese completo del flujo de avance de la solución embólica opacificada. En el grupo NBCA, NBCA se diluyó con aceite yodado (Lipiodol Ultra Fluide, Guerbet, Roissy, Francia) en una proporción de 1:3 a 1:5. Después de enjuagar el microcatéter con solución de dextrosa al 5 %, se administraron cuidadosamente 0,5–2 ml de la mezcla bajo fluoroscopia. [7]. La relación de mezcla, el volumen de inyección y la velocidad se determinaron en función del tamaño del vaso objetivo y el flujo sanguíneo. Después de la inyección de la mezcla, se retiró rápidamente el microcatéter para evitar adherencias de la punta del catéter al vaso. Se preparó un nuevo microcatéter para cada embolización mediante NBCA si había más de un vaso culpable. Después…