Resumen
Antecedentes
La esclerosis sistémica (SSC) es una enfermedad rara de tejido conectivo asociado con enfermedad pulmonar intersticial (ILD) en rápida evolución, lo que impulsa su mortalidad. Se necesitan biomarcadores específicos basados en imágenes asociados con la evolución de la enfermedad pulmonar para ayudar a predecir y cuantificar ILDL.
Métodos
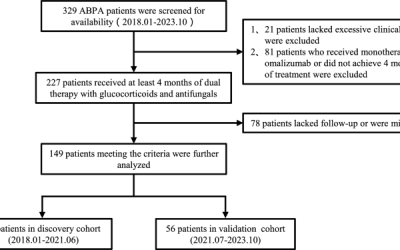
Evaluamos el potencial de un sistema automatizado de cuantificación ILD (ICOLung®) de las tomografías computarizadas en el pecho, para ayudar en la cuantificación y la predicción de la progresión de ILD en SSC-PILD. Utilizamos una cohorte retrospectiva de 75 pacientes con SSC-IDS para evaluar el potencial de la herramienta de cuantificación basada en IA y para correlacionar la cuantificación basada en imágenes con las pruebas de función pulmonar y su evolución a lo largo del tiempo.
Resultados
Evaluamos un grupo de 75 pacientes que padecen SSC-IDL, ya sea limitado o difuso, de los cuales 30 presentaron fibrosis pulmonar progresiva (PPF). Los pacientes que presentaron PPF exhibieron lesiones más extensas (en el% del volumen pulmonar total (TLV)) basados en el análisis de imágenes que aquellos sin PPF: 3.93 (0.36–8.12)* vs. 0.59 (0.09–3.53) respectivamente, mientras que la prueba funcional pulmonar mostró una reducción en la capacidad vital de la fuerza (FVC) (pred%) en pacientes con PPF en comparación con los otros: 77 ± 207 ± 207 ± 207 ± 207 ± 20. 87 ± 19% (p <0.05). Las modificaciones de FVC y la capacidad de difusión de los pulmones para el monóxido de carbono (DLCO) a lo largo del tiempo se correlacionaron con modificaciones de ILD radiológicas longitudinales (r = -0.40, p <0.01; r = -0.40, p <0.01 respectivamente).
Conclusión
La cuantificación automática basada en AI de lesiones de imágenes de CT-CT en SSC-IDL se correlaciona con los parámetros fisiológicos y puede ayudar en la evaluación de la enfermedad. Se necesita una validación multicéntrica clínica adicional para confirmar su potencial en la predicción del resultado del paciente y en el manejo del tratamiento.
Fondo
La esclerosis sistémica (SSC) es una enfermedad rara de tejido conectivo de origen desconocido que afecta a múltiples órganos. Caracterizado por la autoinmunidad, la inflamación de los vasos y la fibrosis de órganos, el SSC se clasifica por la extensión de la fibrosis de la piel en dos patrones: esclerosis sistémica cutánea limitada (LCSSC) y esclerosis sistémica cutánea difusa (DCSSC). Una complicación significativa de SSC es la enfermedad pulmonar intersticial (ILD), que varía de progresión lenta a rápida (1,2,3,4,5). Su clasificación clínica se basa en la extensión de la fibrosis de la piel, que divide a los pacientes en dos patrones principales: esclerosis sistémica cutánea limitada (LCSSC), que se caracteriza por la fibrosis de la piel limitada a los codos y las rodillas; y la esclerosis sistémica cutánea difusa, que involucra áreas proximales, la cara y el tronco además de las áreas distales (6, 7). Una complicación principal de SSC que contribuye a la morbilidad es la aparición de la enfermedad pulmonar intersticial (ILD) (8, 9). El curso clínico de la enfermedad pulmonar intersticial asociada a SSC (SSC-IDL) puede variar desde una enfermedad pulmonar que progresa lentamente hasta una progresión rápida (1). El desafío, como con otros ILD (4), está identificando a los pacientes con alto riesgo de progresión e inicia la intervención terapéutica temprana, incluida la terapia inmunosupresora y/o antifibrótica para limitar la extensión de la enfermedad y el brote clínico (2).
Los biomarcadores son cruciales para cuantificar ILD en SSC, proporcionando información sobre la actividad de la enfermedad, la gravedad, la progresión y la respuesta al tratamiento. Ayudan en la detección temprana, la estratificación del riesgo, distinguen los subtipos de ILD y guía el tratamiento dirigido. La cuantificación radiológica de ILD en la TC de alta resolución (TRC) es vital para monitorear la progresión de la enfermedad, predecir los resultados e identificar a los pacientes para la intervención temprana (10). Sin embargo, la evaluación visual de HRCT en ILD es propensa a una alta variabilidad entre observadores, mala reproducibilidad e insensibilidad relativa a la progresión sutil de la enfermedad en breves períodos de seguimiento. Los modelos de aprendizaje automático mejoran las evaluaciones de HRCT mediante la detección y cuantificación de las anormalidades pulmonares, ofreciendo evaluaciones reproducibles y reduciendo la variabilidad entre observadores. Estos modelos también proporcionan medidas objetivas de respuesta al tratamiento, mejorando el desarrollo de fármacos y la selección de pacientes en ensayos clínicos (11,12,13,14,15,16,17,18,19,20).
En este estudio, investigamos la cuantificación automática basada en IA de anomalías pulmonares intersticiales de HRCT en pacientes con SSC-IDS y sus correlaciones con marcadores clínicos estándar como las pruebas de función pulmonar.
Métodos
Pacientes cohortes
Analizamos retrospectivamente a 75 pacientes con SSC-IDL de la Clínica ILD del Hospital Universitario de Liège (CHU) observados entre el 9 de enero de 2007 y el 30 de septiembre de 2022. Se recopilaron datos demográficos (edad, sexo, IMC, estado de tabaco). Con respecto a la clasificación de esclerosis sistémica, los pacientes fueron clasificados de acuerdo con los criterios ACR/EULLE 2013 para SSC (6) y la distinción de las formas cutáneas en limitado y difuso se hizo de acuerdo con la clasificación de Leroy et al. (7). La sina esclerodermia son pacientes sin enfermedad cutánea con otra afectación de órganos. Con respecto a la clasificación de ILD, los pacientes se clasificaron como fibrosis pulmonar progresiva si cumplían con los criterios de Inbuild (PF-ID), que era la definición utilizada antes de 2022 (21). Los criterios para la progresión fibrótica de ILD fueron, en un período de seguimiento de 24 meses antes del análisis:
-
una disminución relativa en la capacidad vital forzada (FVC) de al menos el 10% del valor predicho;
-
o una disminución relativa en el FVC de 5% a menos del 10% del valor predicho y el empeoramiento de los síntomas respiratorios o una mayor extensión de fibrosis en la tomografía computarizada (HRCT) de alta resolución del tórax;
-
o empeoramiento de los síntomas respiratorios y un mayor grado de fibrosis en HRCT.
Un total de 55 pacientes tenían tomografías computarizadas longitudinales de seguimiento (entre 2 y 4 escaneos), entre los cuales 23 eran pacientes con PF-ILD. El protocolo fue aprobado por el Comité de Ética de Chu Liège (Número belga: B7072020000033) y todos los experimentos se realizaron de acuerdo con las pautas y regulaciones relevantes.
Pruebas de función pulmonar
Las pruebas de la función pulmonar se realizaron en el laboratorio respiratorio de rutina en Chu Liège de acuerdo con las recomendaciones de la Sociedad Respiratoria Europea (ERS) (22). Los volúmenes se expresan en litro (l) (valor absoluto) y como porcentaje de valores normales predichos. El índice Tiffeneau o FEV1/FVC se expresa como porcentaje. La capacidad de difusión de Co (DLCO) y el coeficiente de transferencia de monóxido de carbono (KCO o DLCO / VA) se midieron mediante la técnica de prueba de aliento único (Sistema de analizador Sensor Medics 2400 He / Co, Bilthoven, Países Bajos).
Análisis estadístico
La distribución paramétrica de las variables continuas se describió utilizando medias y desviaciones estándar (DE) y distribuciones no paramétricas se describieron utilizando mediana (rango intercuartil: IQR) expresado como número (% sí). Coeficiente de correlación de Spearman (R) (23) se usó para la correlación entre PFT y los parámetros de imagen (correlación fuerte R> 0.7; moderado 0.3-0.7; bajo <0.3). Prueba t de T de pareja y wilcoxon pareja de pares firmados prueba de rango para variables paramétricas y no paramétricas respectivamente (24) se usaron para el análisis longitudinal. La comparación entre SSC-IDL y SSC-PFILD se analizó mediante prueba t no apareada para FVC y DLCO y mediante prueba de Mann-Whitney para el% de TLV y puntaje de gravedad ((25). Se aceptó un valor de P inferior a 0.05 para la significación estadística. El análisis estadístico se realizó utilizando Tibco Statistica, v. 13.5.0, Tibco Software Inc, Palo Alto, CA, EE. UU. Y Graphs utilizando GraphPad Prism Software versión 9.0.0 para Windows, Software GraphPad, San Diego, California, paquete de software de EE. UU.
Parámetros de imágenes
Todas las imágenes de CT utilizadas en el estudio se adquirieron en uno de los cinco escáneres CT multidetector: Siemens Edge Plus (2), GE Revolution CT (1) y GE BrightSpeed (2). Dado que las imágenes de CT se recopilaron retrospectivamente, no había un protocolo de exploración estandarizado sobre el conjunto de datos completo. Todos los escaneos fueron CT de alta resolución de no contraste (espesor de corte ≤ 1 mm) y adquiridos según el estándar de atención.
Software de Icolung
Empleamos el software Icolung, que realiza la segmentación totalmente automatizada de los pulmones, los lóbulos pulmonares y las anormalidades pulmonares (opacidad del vidrio terrestre y consolidación) consecutivamente utilizando modelos de aprendizaje profundo. Estos modelos de redes neuronales convolucionales se basan en las arquitecturas 2D y 3D U-Net descritas en (26, 27), y fueron entrenados, validados y probados en tomografías computarizadas clínicas, junto con delineaciones a nivel de vóxel de anormalidades pulmonares, creadas por radiólogos expertos. Según las máscaras predichas de los modelos para anormalidades y lóbulos pulmonares, la participación pulmonar en cada lóbulo se calculó como la relación entre el volumen de anormalidad frente al volumen del lóbulo, de la cual se obtuvo una puntuación de gravedad específica del lóbulo (0-5). Los cinco puntajes de gravedad se sumaron en un puntaje de gravedad global (0-25) para el examen CT actual del paciente. Un ejemplo del informe de software se representa en la Fig. 1. La salida del software consistió en el volumen pulmonar total (TLV) (L), las anormalidades pulmonares (combinando la consolidación y las opacidades de vidrio terrestre) (% de TLV), consolidación (% de TLV), opacidades de vidrio terrestre (% TLV) y puntaje de gravedad por paciente.
Fig. 1A) Salida del software Icolung que combina la segmentación pulmonar automatizada general (cuantificación TLV) y la asociación con anormalidades lobar. Análisis 3D de anomalías pulmonares parenquimales: vista coronal que ilustra la segmentación pulmonar automatizada y la visualización de anormalidades. Las anormalidades se cuantifican utilizando icolung después de la segmentación del lóbulo y se representan con una vista coronal convencional. La puntuación de gravedad se basa en cinco lóbulos pulmonares que anotan en una escala de 0 a 5, con 0 que no indica participación (<1%); 1, menos del 5% de participación; 2, 5-25% de participación; 3, 26-49% de participación; 4, 50–75% de participación; y 5, más ...
(Tagstotranslate) Esclerosis sistémica (T) Enfermedad pulmonar intersticial (T) Inteligencia artificial (T) Tomografía calculada (T) Pruebas de función pulmonar (T) Sistema de neumología/respiratorio